farmacotherapeutische groep: geneesmiddelen gebruikt bij diabetes, bloedglucoseverlagende geneesmiddelen, exclusief insulines. ATC-code: A10BK02.
werkingsmechanisme
De SGLT2-transporter, uitgedrukt in de proximale niertubuli, is verantwoordelijk voor het grootste deel van de reabsorptie van gefilterde glucose uit het buislumen., Bij diabetespatiënten is een verhoogde reabsorptie van glucose in de nieren aangetoond, wat kan bijdragen tot aanhoudend verhoogde bloedglucoseconcentraties. Canagliflozine is een oraal actieve remmer van SGLT2. Door SGLT2 te remmen, vermindert canagliflozine de reabsorptie van gefilterde glucose en verlaagt het de renale drempel voor glucose (RTG), waardoor de UGE wordt verhoogd, waardoor verhoogde plasmaconcentraties van glucose door dit insuline-onafhankelijke mechanisme worden verlaagd bij patiënten met type 2-diabetes., De verhoogde UGE met SGLT2-remming vertaalt zich ook in een osmotische diurese, waarbij het diuretisch effect leidt tot een verlaging van de systolische bloeddruk; de toename in UGE resulteert in een verlies van calorieën en daarom een vermindering van het lichaamsgewicht, zoals is aangetoond in studies met patiënten met type 2 diabetes.
de werking van canagliflozine om de UGE te verhogen die de plasmaglucose rechtstreeks verlaagt, is onafhankelijk van insuline., In klinische studies met canagliflozine is een verbetering waargenomen in de beoordeling van het homeostasemodel voor de bètacelfunctie (HOMA-bètacel) en een verbeterde reactie op de insulinesecretie van de bètacel op een gemengde maaltijd.
in Fase 3-studies gaf toediening van canagliflozine 300 mg vóór de maaltijd een grotere afname van de postprandiale glucoseexcursie dan waargenomen met de dosis van 100 mg., Dit effect bij de dosis van 300 mg canagliflozine kan gedeeltelijk te wijten zijn aan lokale remming van intestinale sglt1 (een belangrijk intestinale glucosetransporter) gerelateerd aan voorbijgaande hoge concentraties canagliflozine in het intestinale lumen voorafgaand aan de absorptie van het geneesmiddel (canagliflozine is een remmer met een lage potentie van de sglt1-transporter). Studies hebben geen glucose malabsorptie met canagliflozine aangetoond.,
canagliflozine verhoogt de afgifte van natrium aan de distale tubulus door de SGLT2-afhankelijke glucose-en natriumreabsorptie te blokkeren, waardoor de tubuloglomerulaire feedback toeneemt, wat gepaard gaat met een afname van de intraglomerulaire druk en een afname van hyperfiltratie in preklinische modellen van diabetes en klinische studies.
farmacodynamische effecten
na enkelvoudige en meervoudige orale doses canagliflozine bij patiënten met type 2 diabetes werden dosisafhankelijke afnames van RTG en verhogingen van UGE waargenomen., In Fase 1-studies werd bij patiënten met type 2-diabetes een maximale suppressie van de gemiddelde 24-uurs RTG van ongeveer 13 mmol/l gezien bij een dagelijkse dosis van 300 mg tot ongeveer 4 mmol/L tot 5 mmol/l, wat wijst op een laag risico op door de behandeling geïnduceerde hypoglykemie. De verlagingen van RTG leidden tot verhoogde UGE bij patiënten met type 2 diabetes die werden behandeld met ofwel 100 mg ofwel 300 mg canagliflozine variërend van 77 g/dag tot 119 g/dag in de fase 1-studies; de waargenomen UGE vertaalt zich in een verlies van 308 kcal/dag tot 476 kcal/dag., De afnames in RTG en toenames in UGE hielden aan gedurende een 26 weken durende doseringsperiode bij patiënten met type 2 diabetes. Matige toenames (in het algemeen < 400 mL tot 500 mL) in het dagelijkse urinevolume werden waargenomen die gedurende enkele dagen van toediening afnamen. De uitscheiding van urinezuur in de urine was tijdelijk verhoogd met canagliflozine (toenam met 19% ten opzichte van de uitgangswaarde op dag 1 en toen afnemend tot 6% op dag 2 en 1% op dag 13). Dit ging gepaard met een aanhoudende verlaging van de urinezuurconcentratie in serum van ongeveer 20%.,
in een onderzoek met eenmalige dosis bij patiënten met type 2 diabetes vertraagde behandeling met 300 mg vóór een gemengde maaltijd de absorptie van glucose in de darm en verminderde de postprandiale glucose via zowel een nier-als een niet-niermechanisme.
klinische werkzaamheid en veiligheid
verbetering van de glykemische controle en vermindering van cardiovasculaire en renale morbiditeit en mortaliteit zijn integrale onderdelen van de behandeling van type 2 diabetes.,
glykemische werkzaamheid en veiligheid
in totaal 10.501 patiënten met type 2 diabetes namen deel aan tien dubbelblinde, gecontroleerde klinische werkzaamheids-en veiligheidsstudies die werden uitgevoerd om de effecten van Invokana op de glykemische controle te evalueren. De raciale verdeling was 72% Blank, 16% Aziatisch, 5% Zwart en 8% andere groepen. 17% van de patiënten was Spaans. 58% van de patiënten was man. De patiënten hadden een totale gemiddelde leeftijd van 59,5 jaar (variërend van 21 jaar tot 96 jaar), met 3.135 patiënten ≥ 65 jaar en 513 patiënten ≥ 75 jaar. 58% van de patiënten had een body mass index (BMI) ≥ 30 kg / m2., In het klinisch ontwikkelingsprogramma werden 1.085 patiënten met een baseline eGFR 30 mL/min/1,73 m2 tot < 60 mL/min/1,73 m2 geëvalueerd.
Placebo-gecontroleerde studies
canagliflozine werd onderzocht als monotherapie, duale therapie met metformine, duale therapie met een sulfonylureumderivaat, triple therapie met metformine en een sulfonylureumderivaat, triple therapie met metformine en pioglitazon en als aanvullende therapie met insuline (tabel 4). In het algemeen produceerde canagliflozine klinisch en statistisch significant (p < 0.,001) resultaten t. o. v. placebo in glykemische controle, waaronder HbA1c, het percentage patiënten dat HbA1c < 7% bereikte, verandering ten opzichte van baseline nuchtere plasmaglucose (FPG) en 2 uur postprandiale glucose (PPG). Daarnaast werden dalingen in lichaamsgewicht en systolische bloeddruk waargenomen ten opzichte van placebo.,
bovendien werd canagliflozine onderzocht als drievoudige therapie met metformine en sitagliptine en gedoseerd met een titratieschema met een startdosis van 100 mg en getitreerd naar 300 mg al in week 6 bij patiënten die aanvullende glykemische controle nodig hadden en die een geschikte eGFR hadden en canagliflozine 100 mg verdroegen (tabel 4). Canagliflozine gedoseerd met een titratieschema produceerde klinisch en statistisch significant (p < 0.,001) resultaten t. o. v. placebo in glykemische controle, inclusief HbA1c en verandering ten opzichte van baseline nuchtere plasmaglucose (FPG), en een statistisch significante (p < 0,01) verbetering in het percentage patiënten dat HbA1c < 7% bereikte. Daarnaast werden dalingen in lichaamsgewicht en systolische bloeddruk waargenomen ten opzichte van placebo.,
naast de hierboven gepresenteerde onderzoeken waren de resultaten van de glykemische werkzaamheid die werden waargenomen in een 18 weken durend subonderzoek met een sulfonylureumderivaat en een 26 weken durend onderzoek met een triple therapie met metformine en pioglitazon over het algemeen vergelijkbaar met de resultaten die werden waargenomen in andere onderzoeken.
actief-gecontroleerd onderzoek
canagliflozine werd vergeleken met glimepiride als tweevoudige therapie met metformine en vergeleken met sitagliptine als drievoudige therapie met metformine en een sulfonylureumderivaat (tabel 5)., Canagliflozine 100 mg als tweevoudige therapie met metformine gaf vergelijkbare verlagingen van HbA1c ten opzichte van baseline en 300 mg produceerde superieure (p < 0,05) verlagingen van HbA1c in vergelijking met glimepiride, wat non-inferioriteit aantoont. Een lager deel van de patiënten behandeld met canagliflozine 100 mg (5,6%) en canagliflozine 300 mg (4,9%) kreeg gedurende 52 weken behandeling ten minste één episode/voorval van hypoglykemie ten opzichte van de groep behandeld met glimepiride (34,2%)., In een vergelijkende studie van canagliflozin 300 mg tot 100 mg sitagliptin in triple therapie met metformine en een enz.), canagliflozin aangetoond dat niet-inferieur (p < 0.05) en superior (p < 0.05) reductie in HbA1c ten opzichte van sitagliptin. De incidentie van hypoglykemie episodes/voorvallen met canagliflozine 300 mg en sitagliptine 100 mg was respectievelijk 40,7% en 43,2%. In vergelijking met zowel glimepiride als sitagliptine werden ook significante verbeteringen van het lichaamsgewicht en verlagingen van de systolische bloeddruk waargenomen.,
canagliflozine als initiële combinatietherapie met metformine
canagliflozine werd geëvalueerd in combinatie met metformine als initiële combinatietherapie bij patiënten met type 2 diabetes waarbij dieet en lichaamsbeweging faalden. Canagliflozine 100 mg en canagliflozine 300 mg in combinatie met metformine XR resulteerden in een statistisch significante grotere verbetering van HbA1C in vergelijking met hun respectievelijke canagliflozinedoses (100 mg en 300 mg) alleen of metformine XR alleen (tabel 6).,
speciale populaties
in drie onderzoeken uitgevoerd bij speciale populaties (oudere patiënten, patiënten met een eGFR van 30 mL/min/1,73 m2 tot < 50 mL/min/1,73 m2 en patiënten met of met een hoog risico op cardiovasculaire aandoeningen) werd canagliflozine toegevoegd aan de huidige stabiele diabetesbehandelingen van patiënten (dieet, monotherapie of combinatietherapie).,
ouderen
in totaal 714 patiënten ≥ 55 jaar tot ≤ 80 jaar oud (227 patiënten 65 jaar tot < 75 jaar oud en 46 patiënten 75 jaar tot ≤ 80 jaar oud) met onvoldoende glykemische controle op de huidige diabetesbehandeling (glucoseverlagende geneesmiddelen en/of dieet en lichaamsbeweging) namen gedurende 26 weken deel aan een dubbelblind, placebogecontroleerd onderzoek. Statistisch significante (p < 0,001) veranderingen ten opzichte van baseline HbA1c ten opzichte van placebo van -0,57% en -0.,70% werd waargenomen voor respectievelijk 100 mg en 300 mg (zie rubrieken 4.2 en 4.8).
Patiënten met een eGFR 45 mL/min/1,73 m2 < 60 mL/min/1,73 m2
In een gepoolde analyse van de patiënten (N = 721) met een baseline eGFR 45 mL/min/1,73 m2 < 60 mL/min/1,73 m2, canagliflozin verstrekt klinisch betekenisvolle reductie in HbA1c ten opzichte van placebo, met -0.47% voor canagliflozin 100 mg en -0.52% voor canagliflozin 300 mg. Patiënten met een baseline eGFR 45 mL/min/1,73 m2 tot < 60 mL/min / 1.,73 m2 Behandeld met canagliflozine 100 mg en 300 mg vertoonde gemiddelde verbeteringen in procentuele verandering in lichaamsgewicht ten opzichte van placebo van respectievelijk -1,8% en -2,0%.
de meerderheid van de patiënten met een baseline eGFR 45 mL/min/1,73 m2 tot < 60 mL/min/1,73 m2 kregen insuline en/of een sulfonylureumderivaat (85% )., In overeenstemming met de verwachte toename van hypoglykemie wanneer een geneesmiddel dat niet geassocieerd is met hypoglykemie wordt toegevoegd aan insuline en/of een sulfonylureumderivaat, werd een toename van episodes/voorvallen van hypoglykemie waargenomen wanneer canagliflozine werd toegevoegd aan insuline en/of een sulfonylureumderivaat (zie rubriek 4.8).
nuchtere plasmaglucose
in vier placebogecontroleerde onderzoeken resulteerde behandeling met canagliflozine als monotherapie of add-on therapie met één of twee orale glucoseverlagende geneesmiddelen in gemiddelde veranderingen ten opzichte van baseline in FPG van -1,2 mmol / L naar -1 ten opzichte van placebo.,9 mmol/L voor canagliflozine 100 mg en -1,9 mmol/L tot -2,4 mmol/L voor canagliflozine 300 mg, respectievelijk. Deze verlagingen hielden aan gedurende de behandelingsperiode en waren bijna maximaal na de eerste dag van de behandeling.
postprandiale glucose
bij gebruik van een mixed meal challenge verminderde canagliflozine als monotherapie of add-on therapie met één of twee orale glucoseverlagende geneesmiddelen de postprandiale glucose (PPG) ten opzichte van de uitgangswaarde met -1,5 mmol/L tot -2,7 mmol/L voor canagliflozine 100 mg en -2,1 mmol/L tot -3.,5 mmol/L voor respectievelijk 300 mg, als gevolg van verlagingen van de glucoseconcentratie vóór de maaltijd en verlaagde postprandiale glucoseexcursies.
lichaamsgewicht
canagliflozine 100 mg en 300 mg als monotherapie en als tweevoudige of drievoudige add-on therapie resulteerde in statistisch significante verlagingen van het percentage lichaamsgewicht na 26 weken ten opzichte van placebo., In twee van 52 weken actief-gecontroleerde studies vergelijken canagliflozin te glimepiride en sitagliptin, duurzame en statistisch significante gemiddelde vermindering in het percentage van het lichaamsgewicht voor canagliflozin als add-on therapie voor metformin -4.2% en -4.7% voor canagliflozin 100 mg en 300 mg, respectievelijk, in vergelijking met de combinatie van glimepiride en metformine (1.0%) en -2.5% voor canagliflozin 300 mg in combinatie met metformine en een enz.) in vergelijking met sitagliptin in combinatie met metformine en een enz.) (0.3%).,
een subgroep van patiënten (N = 208) uit het actief-gecontroleerde onderzoek met tweevoudige therapie met metformine die dual energy X-ray densitometrie (DXA) en abdominale computertomografie (CT) scans ondergingen voor evaluatie van de lichaamssamenstelling, toonde aan dat ongeveer twee derde van het gewichtsverlies met canagliflozine te wijten was aan verlies van vetmassa waarbij vergelijkbare hoeveelheden visceraal en abdominaal subcutaan vet verloren gingen. Tweehonderd Elf (211) patiënten uit de klinische studie bij oudere patiënten namen deel aan een substudie naar de lichaamssamenstelling met behulp van een DXA-analyse van de lichaamssamenstelling., Dit toonde aan dat ongeveer twee derde van het gewichtsverlies geassocieerd met canagliflozine te wijten was aan verlies van vetmassa ten opzichte van placebo. Er waren geen betekenisvolle veranderingen in botdichtheid in trabeculaire en corticale regio ‘ s.
bloeddruk
in placebogecontroleerde onderzoeken resulteerde behandeling met canagliflozine 100 mg en 300 mg in gemiddelde verlagingen van de systolische bloeddruk van respectievelijk -3,9 mmHg en -5,3 mmHg in vergelijking met placebo (-0,1 mmHg) en een kleiner effect op de diastolische bloeddruk met gemiddelde veranderingen voor canagliflozine 100 mg en 300 mg van -2,1 mmHg en -2.,5 mmHg, respectievelijk, vergeleken met placebo (-0,3 mmHg). Er was geen noemenswaardige verandering in de hartslag.
patiënten met baseline HbA1c > 10% tot ≤ 12%
een substudie van patiënten met baseline HbA1c > 10% tot ≤ 12% met canagliflozine als monotherapie resulteerde in verlagingen ten opzichte van baseline van HbA1c (niet placebo-aangepast) van -2,13% en -2,56% voor canagliflozine respectievelijk 100 mg en 300 mg.,
cardiovasculaire uitkomsten in het CANVAS-programma
het effect van canagliflozine op cardiovasculaire voorvallen bij volwassenen met diabetes type 2 die een cardiovasculaire (CV) ziekte hadden vastgesteld of risico liepen op CVD (twee of meer CV risicofactoren), werd geëvalueerd in het CANVAS-programma (geïntegreerde analyse van het CANVAS-en het CANVAS-R-onderzoek). Deze onderzoeken waren multicenter, multinationaal, gerandomiseerd, dubbelblind, parallelgroep, met vergelijkbare inclusie-en uitsluitingscriteria en patiëntenpopulaties., Het CANVAS-programma vergeleek het risico op het ervaren van een Major Adverse Cardiovascular Event (MACE) gedefinieerd als de samenstelling van cardiovasculair overlijden, niet-fataal myocardinfarct en niet-fatale beroerte, tussen canagliflozine en placebo op een achtergrond van standaardzorgbehandelingen voor diabetes en atherosclerotische cardiovasculaire aandoeningen.
bij CANVAS werden de proefpersonen willekeurig 1:1:1 toegewezen aan 100 mg canagliflozine, 300 mg canagliflozine, of een overeenkomstige placebo., Bij CANVAS-R werden proefpersonen willekeurig 1:1 toegewezen aan 100 mg canagliflozine of een overeenkomstige placebo, en titratie tot 300 mg was toegestaan (op basis van verdraagbaarheid en glykemische behoeften) na Week 13. Gelijktijdige antidiabetica en atherosclerotische therapieën kunnen worden aangepast, afhankelijk van de standaardzorg voor deze ziekten.
in totaal werden 10.134 patiënten behandeld (4.327 in CANVAS en 5.807 in CANVAS-R; in totaal 4.344 willekeurig toegewezen aan placebo en 5.790 aan canagliflozine) gedurende een gemiddelde blootstellingsduur van 149 weken (223 weken in CANVAS en 94 weken in CANVAS-R). Vitale status werd verkregen voor 99.,6% van de proefpersonen in de studies. De gemiddelde leeftijd was 63 jaar en 64% was man. Zesenzestig procent van de proefpersonen had een voorgeschiedenis van vastgestelde hart-en vaatziekten, met 56% met een voorgeschiedenis van coronaire ziekte, 19% met cerebrovasculaire ziekte, en 21% met perifere vasculaire ziekte; 14% had een voorgeschiedenis van hartfalen.
De gemiddelde HbA1c bij baseline was 8,2% en de gemiddelde duur van diabetes was 13,5 jaar.
uitgangswaarde de nierfunctie was normaal of licht verminderd bij 80% van de patiënten en matig verminderd bij 20% van de patiënten (gemiddelde eGFR 77 mL/min/1,73 m2)., Bij aanvang werden de patiënten behandeld met één of meer antidiabetica waaronder metformine (77%), insuline (50%) en sulfonylureum (43%).
het primaire eindpunt in het CANVAS-programma was de tijd tot het voor het eerst voorkomen van een MACE. Secundaire eindpunten binnen een sequentiële voorwaardelijke hypothese testen waren alle oorzaken mortaliteit en cardiovasculaire mortaliteit.
patiënten in de gepoolde canagliflozinegroepen (gepoolde analyse van canagliflozine 100 mg, canagliflozine 300 mg en canagliflozine verhoogd van 100 mg naar 300 mg) hadden een lager percentage MACE in vergelijking met placebo: 2,69 versus 3.,15 patiënten per 100 patiëntjaren (HR van de gepoolde analyse: 0,86; 95% BI (0,75; 0,97).
Op basis van de Kaplan-Meier-grafiek voor het eerste voorkomen van MACE, die hieronder wordt weergegeven, werd de afname van MACE in de canagliflozinegroep al in Week 26 waargenomen en bleef deze gedurende de rest van het onderzoek behouden (zie Figuur 1).
figuur 1: tijd tot eerste voorkomen van MACE
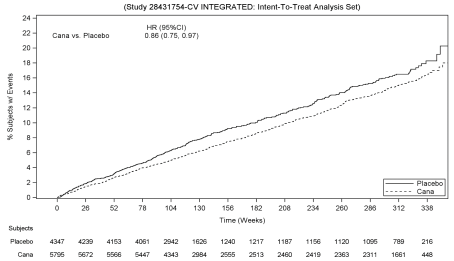
er waren 2011 patiënten met eGFR 30 tot < 60 mL/min / 1,73 m2. De bevindingen van MACE in deze subgroep waren consistent met de algemene bevindingen.,
elke MACE-component droeg positief bij aan de totale samenstelling, zoals weergegeven in Figuur 2. De resultaten voor de doses van 100 mg en 300 mg canagliflozine waren consistent met de resultaten voor de gecombineerde dosisgroepen.
Figuur 2: behandelingseffect voor het primaire samengestelde eindpunt en zijn componenten
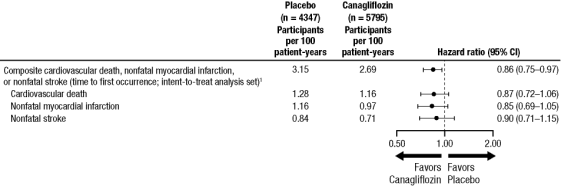
1 p waarde voor superioriteit (2-zijdige) = 0,0158.
mortaliteit door alle oorzaken in het CANVAS-programma
in de gecombineerde canagliflozine-groep was de HR voor mortaliteit door alle oorzaken versus placebo 0,87; 95% BI (0,74; 1,01).,
hartfalen waarvoor ziekenhuisopname nodig was in het CANVAS-programma verminderde
canagliflozine het risico op hartfalen waarvoor ziekenhuisopname nodig was in vergelijking met placebo (HR: 0,67; 95% BI (0,52; 0,87)).
Niereindpunten in het CANVAS-programma
Nieruitkomsten in de CREDENCE-studie
het effect van canagliflozine 100 mg op renale voorvallen bij volwassenen met diabetes type 2 en diabetische nierziekte (DKD) met een geschatte glomerulaire filtratiesnelheid (eGFR) 30 tot< 90 mL/min / 1.,73 m2 en albuminurie (300 tot 5000 mg/g creatinine), werd geëvalueerd in de canagliflozine en renale voorvallen bij Diabetes met gevestigde nefropathie Clinical Evaluation Trial (CREDENCE). Dit was een multicenter, multinationaal, gerandomiseerd, dubbelblind, gebeurtenisgestuurd, placebogecontroleerd onderzoek met parallelle groepen., In het CREDENCE-onderzoek werd het risico op het optreden van DKD, gedefinieerd als de samenstelling van terminale nierziekte, verdubbeling van serumcreatinine en renale of cardiovasculaire sterfte, vergeleken tussen 100 mg canagliflozine en placebo op basis van standaardbehandeling voor DKD, waaronder angiotensin-converting enzyme inhibitor (ACE-remmer) of angiotensin receptorblokker (ARB). Canagliflozine 300 mg werd in dit onderzoek niet onderzocht.,
in CREDENCE werden proefpersonen willekeurig 1:1 toegewezen aan 100 mg canagliflozine of placebo, gestratificeerd per screening eGFR 30 aan <45, 45 aan <60, 60 aan <90 mL/min / 1,73 m2. De behandeling met canagliflozine 100 mg werd voortgezet bij patiënten tot de start van de dialyse of in het geval van niertransplantatie.
in totaal werden 4.397 patiënten behandeld en blootgesteld gedurende gemiddeld 115 weken. De gemiddelde leeftijd was 63 jaar en 66% was man.
De gemiddelde baseline HbA1c was 8.,De meest frequent gebruikte antihyperglykemische middelen (AHA) bij aanvang waren insuline (65,5%), biguaniden (57,8%) en sulfonylureumderivaten (28,8%). Bijna alle proefpersonen (99,9%) kregen ACE-remmers of ARB bij randomisatie. Ongeveer 92% van de proefpersonen kreeg cardiovasculaire therapieën (zonder ACE-remmers/ARBs) bij aanvang, waarbij ongeveer 60% een antitrombotisch middel (inclusief acetylsalicylzuur) gebruikte en 69% statines.
De gemiddelde EGFR bij aanvang was 56,2 mL / min / 1.,73 m2 en ongeveer 60% van de populatie had een baseline eGFR van < 60 mL/min/1,73 m2. Het percentage proefpersonen met eerder cardiovasculaire ziekte was 50,4%; 14,8% had een voorgeschiedenis van hartfalen.
het primaire samengestelde eindpunt in de CREDENCE-studie was de tijd tot het eerste optreden van ESKD (gedefinieerd als een eGFR < 15 mL/min/1,73 m2, aanvang van chronische dialyse of niertransplantatie), verdubbeling van het serumcreatinine en overlijden via de nieren of CV.,
canagliflozine 100 mg verminderde significant het risico op het eerste optreden van het primaire samengestelde eindpunt van ESKD, verdubbeling van serumcreatinine en overlijden door nier-of CV-oorzaak (zie Figuur 4). Het behandelingseffect was consistent in alle subgroepen, waaronder alle drie de eGFR-strata en patiënten met of zonder voorgeschiedenis van cardiovasculaire ziekte.
gebaseerd op de Kaplan-Meier-plot voor de tijd tot het eerste optreden van het primaire samengestelde eindpunt dat hieronder wordt getoond, was het behandelingseffect duidelijk vanaf week 52 met canagliflozine 100 mg en bleef behouden tot het einde van de studie (zie Figuur 3).,
canagliflozine 100 mg verminderde significant het risico op cardiovasculaire secundaire eindpunten, zoals weergegeven in Figuur 4.
Figuur 3: CREDENCE: tijd tot het eerste optreden van het primaire samengestelde eindpunt
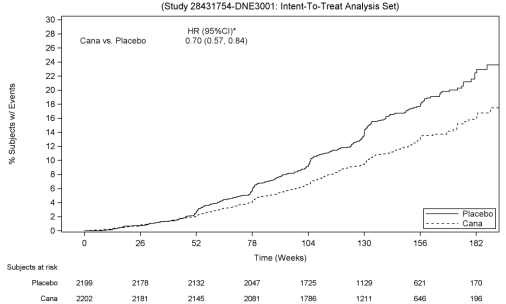
* 95% RCI (herhaald betrouwbaarheidsinterval) voor het primaire eindpunt met familiegewijs type I foutenpercentage gecontroleerd op een 2-zijdige significantieniveau van 0,05.,
Figuur 4: behandelingseffect voor het primaire samengestelde eindpunt en de componenten en secundaire eindpunten
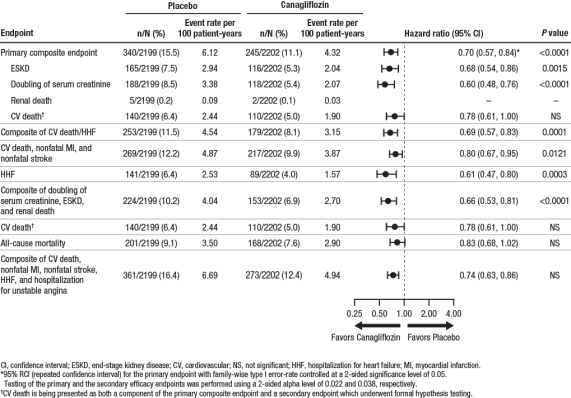
zoals weergegeven in Figuur 5, vertoonde de eGFR bij met placebo behandelde patiënten een progressieve lineaire afname in de tijd; de canagliflozinegroep daarentegen vertoonde een acute afname in Week 3, gevolgd door een verzwakte afname in de tijd; na Week 52 was de gemiddelde LS-afname in eGFR kleiner in de canagliflozinegroep dan in de placebogroep en het behandelingseffect bleef behouden tot het einde van de behandeling.,
Figuur 5: LS gemiddelde verandering ten opzichte van baseline in eGFR in de tijd (on-treatment analysis set)
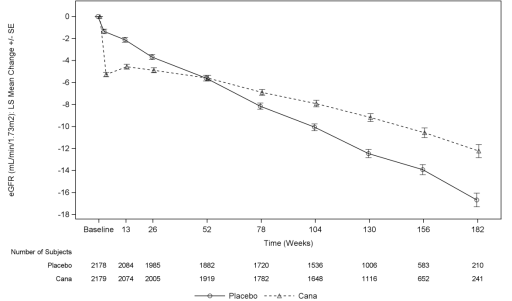
in CREDENCE was het incidentiepercentage voor niergerelateerde bijwerkingen lager in de canagliflozine 100 mg groep vergeleken met de placebogroep (5,71 en 7,91 per 100 patiëntjaren in respectievelijk canagliflozine 100 mg en placebo).
pediatrische patiënten
het Europees Geneesmiddelenbureau heeft besloten tot uitstel van de verplichting voor de fabrikant om de resultaten in te dienen van onderzoek met canagliflozine in een of meer subgroepen van pediatrische patiënten met type 2 diabetes (zie rubriek 4.,2 voor informatie over pediatrisch gebruik).