Farmakoterapeutisk gruppe: Legemidler som brukes ved diabetes, blodglukose senkende medikamenter, unntatt insulins. ATC-kode: A10BK02.
virkningsmekanisme
SGLT2 transporter, uttrykt i den proksimale tubuli renal, er ansvarlig for de fleste av reabsorpsjon av filtrert glukose fra den tubulære lumen., Pasienter med diabetes har vist seg å ha forhøyet nedsatt glukose reabsorpsjon som kan bidra til vedvarende forhøyet blodsukker konsentrasjoner. Canagliflozin er et oralt aktivt hemmer av SGLT2. Ved å hemme SGLT2, canagliflozin reduserer reabsorpsjon av filtrert glukose og senker nedsatt terskel for glukose (RTG), og dermed øker UGE, senke forhøyet plasma glukose konsentrasjoner av dette insulin-uavhengig mekanisme hos pasienter med type 2 diabetes., Den økte UGE med SGLT2 hemming også oversettes til et osmotisk diurese, med vanndrivende effekt som fører til en reduksjon i systolisk blodtrykk; økningen i UGE resulterer i et tap av kalorier og dermed en reduksjon i kroppsvekt, som har vært påvist i studier av pasienter med type 2 diabetes.
Canagliflozin er tiltak for å øke UGE direkte senke plasma-glukose er uavhengig av insulin., Forbedring i homeostase modell vurdering for beta-celle funksjon (HOMA beta-celle) og forbedret beta-celle insulin sekresjon respons til et blandet måltid utfordringen har vært observert i kliniske studier med canagliflozin.
I fase 3-studier, pre-måltid administrasjon av canagliflozin 300 mg gitt en større reduksjon i postprandial glukose utflukt enn observert med 100 mg dose., Denne effekten på 300 mg dose av canagliflozin kan delvis skyldes lokale hemming av intestinal SGLT1 (en viktig intestinal glukose transporter) knyttet til forbigående høye konsentrasjoner av canagliflozin i tarmen lumen før legemiddel absorpsjon (canagliflozin er en lav potens inhibitor av SGLT1 transporter). Studier har vist ingen glukose malabsorpsjon med canagliflozin.,
Canagliflozin øker levering av natrium til den distale tubule ved å blokkere SGLT2 avhengige av glukose og natrium reabsorpsjon og dermed øke tubuloglomerular tilbakemeldinger, som er forbundet med en reduksjon i intraglomerular blodtrykk og en nedgang i hyperfiltration i prekliniske modeller av diabetes og kliniske studier.
Farmakodynamiske effekter
Følgende enkle og flere orale doser av canagliflozin til pasienter med type 2 diabetes, doseavhengig reduksjon i RTG og øker i UGE ble observert., Fra en startverdi av RTG av ca 13 mmol/L, maksimal undertrykkelse av 24-timers mener RTG ble sett med 300 mg daglig dose til ca 4 mmol/L til 5 mmol/L hos pasienter med type 2 diabetes i fase 1 studier, noe som tyder på en lav risiko for behandling-indusert hypoglykemi. Reduksjonene i RTG førte til økt UGE i personer med type 2 diabetes behandlet med enten 100 mg eller 300 mg canagliflozin alt fra 77 g/dag til 119 g/dag over fase 1-studier; den UGE observert oversettes til et tap av 308 kcal/dag for å 476 kcal/dag., Reduksjonene i RTG og øker i UGE var opprettholdes over en 26-uke dosering periode hos pasienter med type 2 diabetes. Moderat økning (vanligvis < 400 mL 500 mL) i daglig urinvolum ble sett på som svekket over flere dager etter dosering. Utskillelsen av urinsyre utskillelse var forbigående økt med canagliflozin (økte med 19% i forhold til baseline på dag 1, og deretter dempe til 6% på dag 2 og 1% på dag 13). Dette ble fulgt av en vedvarende reduksjon i serum urinsyre konsentrasjon på ca 20%.,
I en single-dose studie hos pasienter med type 2 diabetes, behandling med 300 mg før et blandet måltid forsinket intestinal glukose absorpsjon og redusert postprandial glukose gjennom både en nyre og en ikke-nyre-mekanisme.
Klinisk effekt og sikkerhet
Forbedring av glykemisk kontroll og reduksjon av hjerte-og nyre-sykelighet og dødelighet er en integrert del av behandlingen av type 2 diabetes.,
Glykemiske effekt og sikkerhet
En total av 10,501 pasienter med type 2 diabetes deltok i ti dobbelt-blind, kontrollert klinisk effekt og sikkerhet studier utført for å evaluere effekten av Invokana på glykemisk kontroll. Den etniske fordelingen var 72% Hvite, 16% Asiater, 5% Sort, og 8% andre grupper. 17% av pasientene var Spanske. 58% av pasientene var menn. Pasientene hadde en samlet gjennomsnittlig alder av 59.5 år (range 21 år til 96 år), med 3,135 pasienter ≥ 65 år og 513 pasienter ≥ 75 år. 58% av pasientene hadde en body mass index (BMI) ≥ 30 kg/m2., I den kliniske utviklingsprogram, 1,085 pasienter med baseline eGFR 30 mL/min/1.73 m2 til < 60 mL/min/1.73 m2 ble evaluert.
Placebo-kontrollerte studier
Canagliflozin ble studert som monoterapi, dual behandling med metformin, dual behandling med et sulphonylurea, trippel behandling med metformin og et sulphonylurea, trippel behandling med metformin og pioglitazon, og som en add-on behandling med insulin (tabell 4). Generelt, canagliflozin produsert klinisk og statistisk signifikant (p < 0.,001) resultater i forhold til placebo i glykemiske kontroll, inkludert, HbA1c, andel av pasientene som oppnår HbA1c < 7%, endring fra baseline fastende plasma glukose (FPG), og 2-timers postprandial glukose (PPG). I tillegg til en reduksjon i kroppsvekt og systolisk blodtrykk i forhold til placebo ble observert.,
Videre, canagliflozin ble studert som trippel behandling med metformin og sitagliptin og doseres med en titrering regime, med utgangspunkt i dose av 100 mg og titrated til 300 mg så tidlig som i uke 6 i pasienter som krever ekstra glykemiske kontroll som hadde riktig eGFR og var tolerer canagliflozin 100 mg (tabell 4). Canagliflozin dosert med en titrering diett produsert klinisk og statistisk signifikant (p < 0.,001) resultater i forhold til placebo i glykemiske kontroll, inkludert HbA1c og endring fra baseline fastende plasma glukose (FPG), og en statistisk signifikant (p < 0.01) forbedring i andelen av pasientene som oppnår HbA1c < 7%. I tillegg til en reduksjon i kroppsvekt og systolisk blodtrykk i forhold til placebo ble observert.,
I tillegg til studiene som er presentert ovenfor, glykemiske effekt resultatene som ble observert i en 18-uke dual terapi sub-studie med en sulphonylurea og en 26-uke trippel terapi studie med metformin og pioglitazon var generelt sett sammenlignbare med de som er observert i andre studier.
Aktiv-kontrollerte studier
Canagliflozin ble sammenlignet med glimepiride som dual behandling med metformin og i forhold til sitagliptin som trippel behandling med metformin og et sulphonylurea (tabell 5)., Canagliflozin 100 mg som dual behandling med metformin produsert tilsvarende reduksjon i HbA1c fra baseline og 300 mg produsert superior (p < 0.05) reduksjon i HbA1c i forhold til glimepiride, og dermed demonstrerer ikke-underlegenhet. En lavere andel av pasientene behandlet med canagliflozin 100 mg (5.6%) og canagliflozin 300 mg (4.9%) hadde opplevd minst én episode/tilfelle av hypoglykemi over 52 uker av behandlingen i forhold til gruppen behandlet med glimepiride (34.2%)., I en studie som sammenlignet canagliflozin 300 mg til sitagliptin 100 mg i trippel behandling med metformin og et sulphonylurea, canagliflozin demonstrert ikke-dårligere enn (p < 0.05) og superior (p < 0.05) reduksjon i HbA1c i forhold til sitagliptin. Forekomsten av hypoglykemi episoder/hendelser med canagliflozin 300 mg og sitagliptin 100 mg var 40.7% og 43.2%, henholdsvis. Betydelige forbedringer i kroppen vekt og reduksjon i systolisk blodtrykk i forhold til både glimepiride og sitagliptin ble også observert.,
Canagliflozin som første kombinasjonsbehandling med metformin
Canagliflozin ble evaluert i kombinasjon med metformin som første kombinasjon terapi hos pasienter med type 2 diabetes sviktende kosthold og mosjon. Canagliflozin 100 mg og canagliflozin 300 mg i kombinasjon med metformin XR resulterte i en statistisk signifikant større bedring i HbA1C i forhold til deres respektive canagliflozin doser (100 mg og 300 mg) alene eller metformin XR alene (tabell 6).,
Spesielle populasjoner
I tre studier utført i spesielle populasjoner (eldre pasienter, pasienter med eGFR 30 mL/min/1.73 m2 til < 50 mL/min/1.73 m2 og pasienter med eller høy risiko for hjerte-og karsykdommer), canagliflozin ble lagt til pasientenes nåværende stabile diabetes behandlinger (kosthold, monoterapi, eller en kombinasjon terapi).,
Eldre
totalt 714 pasienter ≥ 55 år for å ≤ 80 år (227 pasienter 65 år til < 75 år og 46 pasienter på 75 år for å ≤ 80 år) med utilstrekkelig glykemisk kontroll på gjeldende behandling av diabetes (glukose-senke legemidler og/eller kosthold og mosjon) har deltatt i en dobbel-blind, placebo-kontrollert studie over 26 uker. Statistisk signifikant (p < 0.001) endring fra baseline HbA1c i forhold til placebo av -0.57% og -0.,70% ble observert for 100 mg og 300 mg, henholdsvis (se avsnittene 4.2 og 4.8).
Pasienter med eGFR 45 mL/min/1.73 m2 til < 60 mL/min/1.73 m2
I en samlet analyse av pasienter (N = 721) med en baseline eGFR 45 mL/min/1.73 m2 til < 60 mL/min/1.73 m2, canagliflozin gitt klinisk meningsfull reduksjon i HbA1c i forhold til placebo, med -0.47% for canagliflozin 100 mg og -0.52% for canagliflozin 300 mg. Pasienter med baseline eGFR 45 mL/min/1.73 m2 til < 60 mL/min/1.,73 m2 behandlet med canagliflozin 100 mg og 300 mg utstilt betyr forbedringer i prosent endring i kroppsvekt i forhold til placebo av -1.8% og -2.0%, henholdsvis.
flertallet av pasienter med baseline eGFR 45 mL/min/1.73 m2 til < 60 mL/min/1.73 m2 var på insulin og/eller en sulphonylurea (85% )., I tråd med den forventede økningen av hypoglykemi når et legemiddel som ikke er knyttet til hypoglykemi er lagt til insulin og/eller sulphonylurea, en økning på hypoglykemi episoder/hendelser som ble sett på når canagliflozin ble lagt til insulin og/eller en sulphonylurea (se avsnitt 4.8).
Fastende plasma-glukose
I fire placebo-kontrollerte studier, behandling med canagliflozin som monoterapi eller add-on behandling med en eller to oral glukose-senke legemidler som resulterte i gjennomsnittlig endring fra baseline i forhold til placebo i FPG av -1.2 mmol/L -1.,9 mmol/L for canagliflozin 100 mg og -1.9 mmol/L for å -2.4 mmol/L for canagliflozin 300 mg, resp. Disse reduksjonene ble oppholdt i løpet av behandlingsperioden og i nærheten maksimal etter første dag av behandlingen.
Postprandial glukose
ved Hjelp av et blandet måltid utfordring, canagliflozin som monoterapi eller add-on behandling med en eller to oral glukose-senke legemidler redusert postprandial glukose (PPG) fra baseline i forhold til placebo ved -1.5 mmol/L for å -2.7 mmol/L for canagliflozin 100 mg og -2.1 mmol/L for å -3.,5 mmol/L for 300 mg, henholdsvis på grunn av reduksjoner i pre-måltid glukose konsentrasjon og redusert postprandial glukose utflukter.
kroppsvekt
Canagliflozin 100 mg og 300 mg som monoterapi og som dobbel eller trippel add-on behandling resulterte i en statistisk signifikant reduksjon i andelen av kroppsvekt på 26 uker i forhold til placebo., I to 52-ukers aktiv-kontrollerte studier som sammenlignet canagliflozin å glimepiride og sitagliptin, vedvarende og statistisk signifikant midlere reduksjon i prosent av kroppsvekt for canagliflozin som add-on til terapi metformin var -4.2% og -4.7% for canagliflozin 100 mg og 300 mg, henholdsvis i forhold til kombinasjonen av glimepiride og metformin (1,0%) og -2.5% for canagliflozin 300 mg i kombinasjon med metformin og et sulphonylurea i forhold til sitagliptin i kombinasjon med metformin og et sulphonylurea (0.3%).,
En undergruppe av pasienter (N = 208) fra aktiv-kontrollerte dual terapi studie med metformin som gjennomgikk dual energy X-ray densitometry (DXA) og abdominal computertomografi (CT) skanner for evaluering av kroppssammensetning vist at omtrent to tredjedeler av vekttap med canagliflozin var på grunn av tap av fettmasse med tilsvarende beløp av visceral og abdominal underhudsfett å være tapt. To hundre og elleve (211) pasienter fra kliniske studier hos eldre pasienter deltok i en kroppssammensetning substudy med DXA kroppssammensetning analyse., Dette viste at om lag to tredjedeler av vekt-tap forbundet med canagliflozin var på grunn av tap av fettmasse i forhold til placebo. Det var ikke noe meningsfylt endringer i bentetthet i trabekulært og kortikale områder.
blodtrykk
I placebo-kontrollerte studier, behandling med canagliflozin 100 mg og 300 mg resulterte i gjennomsnittlig reduksjon i systolisk blodtrykk på -3.9 mmHg og -5.3 mmHg, henholdsvis i forhold til placebo (-0.1 mmHg) og en mindre effekt på diastolisk blodtrykk med bety endringer for canagliflozin 100 mg og 300 mg -2.1 mmHg og -2.,5 mmHg, henholdsvis i forhold til placebo (-0.3 mmHg). Det var ingen merkbar endring i hjerterytmen.
Pasienter med baseline HbA1c > 10% ≤ 12%
En substudy av pasienter med baseline HbA1c > 10% ≤ 12% med canagliflozin som monoterapi resulterte i reduksjon fra baseline i HbA1c (ikke placebo-justert) av -2.13% og -2.56% for canagliflozin 100 mg og 300 mg, resp.,
Kardiovaskulære utfall i LERRETET Program
effekten av canagliflozin på kardiovaskulære hendelser hos voksne med type 2 diabetes som hadde etablert hjerte-og (CV) sykdom eller var i fare for CVD (to eller flere CV risikofaktorer), ble evaluert i LERRET-Programmet (integrert analyse av LERRETET og LERRET-R studien). Disse studiene var multi-senter, multi-nasjonale, randomiserte, dobbelt-blind, parallell gruppe, med lignende inklusjon-og eksklusjonskriterier og pasientpopulasjoner., LERRETET Program sammenlignet risikoen for å oppleve en Stor Ugunstig Kardiovaskulær Hendelse (SEPTER) definert som kompositt for kardiovaskulær død, nonfatal myocardial infarction og nonfatal hjerneslag, mellom canagliflozin og placebo på bakgrunn av standarden på omsorg behandlinger for diabetes og aterosklerotisk kardiovaskulær sykdom.
I LERRET, pasienter ble randomisert 1:1:1 til canagliflozin 100 mg, canagliflozin 300 mg, eller tilsvarende placebo., I CANVAS-R, pasienter ble randomisert 1:1 til canagliflozin 100 mg eller matchende placebo, og titrering til 300 mg var tillatt (basert på toleranse og glykemiske behov) etter Uke 13. Samtidig antidiabetic og aterosklerotisk behandlingsformer kan bli justert i henhold til standard behandling for disse sykdommene.
En total av 10,134 pasienter ble behandlet (4,327 i LERRET og 5,807 i CANVAS-R; totalt 4,344 randomisert til placebo og 5,790 å canagliflozin) for en gjennomsnittlig eksponering varighet av 149 uker (223 uker i LERRET og 94 uker på LERRET-R). Vital status ble innhentet for 99.,6% av fag på tvers av studiene. Gjennomsnittsalderen var 63 år og 64% var menn. Seksti-seks prosent av pasientene hadde en historie med etablert hjerte-og karsykdom, med 56% som har en historie med koronar sykdom, 19% med cerebrovaskulær sykdom, og 21% med perifer vaskulær sykdom; 14% hadde en historie av hjertesvikt.
The mean HbA1c ved baseline var på 8,2% og gjennomsnittlig varighet av diabetes var 13.5 år.
Baseline nyrefunksjon var normal eller mildt nedsatt i 80% av pasienter og moderat nedsatt i 20% av pasientene (mean eGFR 77 mL/min/1.73 m2)., Ved baseline, pasienter ble behandlet med ett eller flere antidiabetic legemiddel inkludert metformin (77%), insulin (50%), og sulfonylurea (43%).
Den primære endepunktet i LERRET-Programmet ble det tid til første forekomst av et SEPTER. Sekundære endepunkter i en sekvensiell betinget hypotesetesting var alle-gi dødelighet og kardiovaskulær dødelighet.
Pasienter i den sammenslåtte canagliflozin grupper (samlet analyse av canagliflozin 100 mg, canagliflozin 300 mg, og canagliflozin opp-titrated fra 100 mg til 300 mg) hadde en lavere pris med TÅREGASS i forhold til placebo: 2.69 mot 3.,15 pasienter per 100 pasient-årene (HR av samlet analyse: 0.86; 95% CI (0.75, 0.97).
Basert på Kaplan-Meier tomten til den første forekomsten av SEPTER, som vist nedenfor, reduksjon i SEPTER i canagliflozin gruppen ble observert så tidlig som i Uke 26 og ble opprettholdt gjennom resten av studiet (se Figur 1).
Figur 1: Tid til første forekomst av MACE
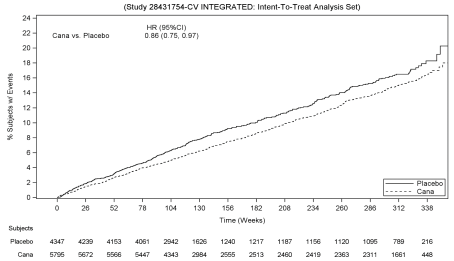
Det var 2,011 pasienter med eGFR 30 til < 60 mL/min/1.73 m2. Den MACE funn i denne undergruppen var i samsvar med den generelle funn.,
Hver MACE komponent, bidro positivt til den generelle kompositt, som vist i Figur 2. Resultatene for de 100 mg og 300 mg canagliflozin doser var i samsvar med resultatene for den kombinerte dose grupper.
Figur 2: Behandling effekt for den primære kompositt endepunkt og dens komponenter
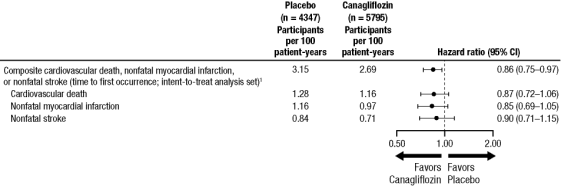
1 P-verdi for overlegenhet (2-sidig) = 0.0158.
Alle-gi dødelighet i LERRETET Program
I den kombinerte canagliflozin gruppe, HR-for all-cause mortality versus placebo var 0.87; 95% CI (0.74, 1.01).,
hjertesvikt som krever sykehusinnleggelse i LERRETET Program
Canagliflozin reduserte risikoen for hjertesvikt som krever sykehusinnleggelse i forhold til placebo (HR: 0.67; 95% CI (0.52, 0.87)).
Nedsatt endepunkter i LERRETET Program
Nedsatt resultater i den TRO studie
effekten av canagliflozin 100 mg på nyre-hendelser hos voksne med type 2 diabetes og diabetisk nyresykdom (DKD) med anslått glomerular filtration rate (eGFR) 30 til < 90 mL/min/1.,73 m2 og albuminuria ( 300 til 5000 mg/g kreatinin), ble evaluert i Canagliflozin og Nedsatt Hendelser i Diabetes med Etablerte Nefropati Klinisk Evaluering Trial (TROVERDIGHET). Dette var en multi-senter, multi-nasjonale, randomiserte, dobbelt-blind, event-drevet, placebo-kontrollert, parallell-gruppe studie., Den TROVERDIGHET studie har sammenlignet risikoen for å oppleve DKD definert som sammensatt av end-stage nyresykdom, en dobling av serum-kreatinin, og nyre eller hjerte-og død, mellom canagliflozin 100 mg og placebo på bakgrunn av standarden på omsorg behandlinger for DKD, inkludert angiotensin-converting enzyme inhibitor (ACEi) eller angiotensin reseptor blokker (ARB). Canagliflozin 300 mg ble ikke undersøkt i denne studien.,
I TRO, pasienter ble randomisert 1:1 til canagliflozin 100 mg eller placebo, stratifisert med screening eGFR 30 til <45, 45 <60, 60 til <90 mL/min/1.73 m2. Behandling med canagliflozin 100 mg ble videreført i pasienter før oppstart av dialyse eller i tilfelle av nyre-transplantasjon.
En total av 4,397 pasienter ble behandlet og utsatt for et gjennomsnitt på 115 uker. Gjennomsnittsalderen var 63 år og 66% var menn.
Det betyr baseline HbA1c var 8.,3% og baseline median urin albumin/kreatinin var 927 mg/g. De mest hyppige antihyperglycaemic agenter (AHA) som brukes ved baseline var insulin (65.5%), biguanides (57.8%), og sulfonylurea (28.8%). Nesten alle fag (99.9%) var på ACEi eller ARB på randomisation. Om 92% av pasientene var på hjerte-og behandlingsformer (ikke inkludert ACEi/ARBs) ved baseline, med ca 60% for å ta en anti-trombotisk agent (inkl. acetylsalisylsyre) og 69% på statiner.
Det betyr baseline eGFR var 56.2 mL/min/1.,73 m2, og ca 60% av befolkningen hadde en baseline av eGFR < 60 mL/min/1.73 m2. Andelen av personer med før CV-sykdom var 50.4%; 14.8% hadde en historie av hjertesvikt.
Den primære kompositt endepunkt i den TRO studien ble det tid til første forekomst av ESKD (definert som en eGFR < 15 mL/min/1.73 m2, initiering av kronisk dialyse eller nyre-transplantasjon), dobling av serum-kreatinin, og nyre-eller CV død.,
Canagliflozin 100 mg betydelig redusert risikoen for første forekomst av primære kompositt endepunktet for ESKD, dobling av serum-kreatinin, og nyre-eller CV død (se Figur 4). Behandling effekten var konsekvent på tvers av undergrupper, inkludert alle de tre eGFR strata og fag med eller uten en historie med CV sykdom.
Basert på Kaplan-Meier tomt for tiden til første forekomst av primære kompositt endepunkt er vist nedenfor, behandling effekten var tydelig fra og med Uke 52 med canagliflozin 100 mg og ble opprettholdt gjennom slutten av studien (se Figur 3).,
Canagliflozin 100 mg betydelig redusert risiko for hjerte-og sekundære endepunkter, som vist i Figur 4.
Figur 3: TROVERDIGHET: Tid til første forekomst av primære kompositt endepunkt
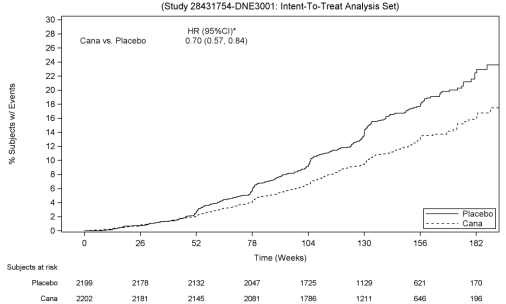
* 95% RCI (Gjentatt konfidensintervall) for de primære endepunkt med familie-messig type i-feil-rate kontrollert av en 2-sidig betydning nivå på 0,05.,
Figur 4: Behandling effekt for den primære kompositt endepunkt og dens komponenter og sekundære endepunkter
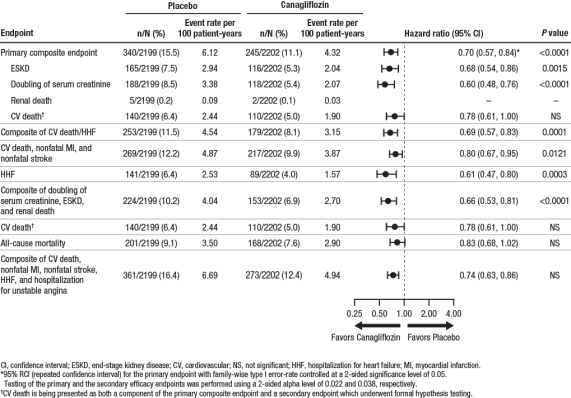
Som vist i Figur 5, eGFR i placebo-behandlede pasienter viste en progressiv lineær nedgang over tid, i kontrast til canagliflozin gruppen viste en akutt reduksjon i Uke 3, etterfulgt av en svekket nedgang over tid; etter Uke 52, LS mener nedgang i eGFR var mindre i canagliflozin gruppen enn i placebogruppen, og behandling effekten ble opprettholdt gjennom slutten av behandlingen.,
Figur 5: LS bety endring fra baseline i eGFR over tid (etter-behandling analyse sett)
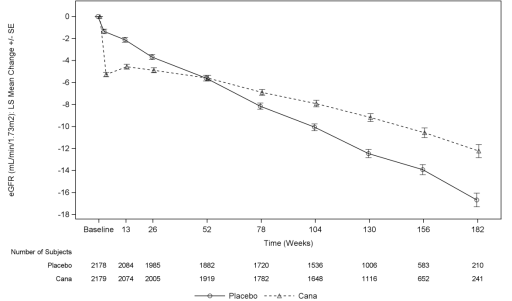
I TRO, i insidensrate for nyre-relaterte bivirkninger var lavere i canagliflozin 100 mg gruppe sammenlignet med placebo-gruppen (5.71 og 7.91 per 100 pasient-årene i canagliflozin 100 mg og placebo, henholdsvis).
Paediatric befolkningen
Det Europeiske legemiddelkontoret har utsatt plikten til å sende inn resultatene av studier med canagliflozin i ett eller flere undergrupper av paediatric befolkningen i type 2 diabetes (se kapittel 4.,2 for informasjon om paediatric bruk).