The chemical element palladium is classed as a transition metal. It was discovered in 1803 by William H. Wollaston.

Data Zone
| Classification: | Palladium is a transition metal |
| Color: | silvery-white |
| Atomic weight: | 106.,4 |
| State: | solid |
| Melting point: | 1555 oC, 1828 K |
| Boiling point: | 2960 oC, 3233 K |
| Electrons: | 46 |
| Protons: | 46 |
| Neutrons in most abundant isotope: | 60 |
| Electron shells: | 2,8,18,18 |
| Electron configuration: | 4d10 |
| Density @ 20oC: | 12.,02 g/cm3 |
Show more, including: Heats, Energies, Oxidation,
Reactions, Compounds, Radii, Conductivities
| Atomic volume: | 8.9 cm3/mol |
| Structure: | ccp (cubic close-packed) |
| Hardness: | 4.8 mohs |
| Specific heat capacity | 0.24 J g-1 K-1 |
| Heat of fusion | 17.60 kJ mol-1 |
| Heat of atomization | 378 kJ mol-1 |
| Heat of vaporization | 357.,0 kJ mol-1 |
| 1st ionization energy | 804.7 kJ mol-1 |
| 2nd ionization energy | 1894 kJ mol-1 |
| 3rd ionization energy | 3177.2 kJ mol-1 |
| Electron affinity | 53.7 kJ mol-1 |
| Minimum oxidation number | 0 |
| Min. common oxidation no. | 0 |
| Maximum oxidation number | 4 |
| Max. common oxidation no. | 4 |
| Electronegativity (Pauling Scale) | 2.,2 |
| Polarisierbarkeit Volumen | 4., |
| Oxide(s) | PdO, PdO2 |
| Hydride(s) | PdH2 |
| Chloride(s) | PdCl2 |
| Atomic radius | 137 pm |
| Ionic radius (1+ ion) | 73 pm |
| Ionic radius (2+ ion) | 78pm |
| Ionic radius (3+ ion) | 90 pm |
| Ionic radius (1- ion) | – |
| Ionic radius (2- ion) | – |
| Ionic radius (3- ion) | – |
| Thermal conductivity | 71.,8 W m-1 K-1 |
| Elektrische Leitfähigkeit | 10 x 106 S m-1 |
| Einfrieren/Schmelzpunkt: | 1555 oC, 1828 K |

Nanoskaligen Bild von palladium-Metall-Oberfläche. Bild. – Ref.(1)
Entdeckung von Palladium
Palladium wurde 1803 in London vom englischen Chemiker William H. Wollaston (der auch Rhodium im selben Jahr entdeckte) entdeckt.,
Er untersuchte die Reste von Platin nach dem Auflösen in Aqua regia, einer konzentrierten Lösung von Salz-und Salpetersäuren. Anschließend isolierte er Palladium in einer Reihe chemischer Reaktionen und erhitzte schließlich Palladium-Cyanid, um Palladium-Metall zu extrahieren.
Wollaston teilte seine Entdeckung auf unkonventionelle Weise mit. Er hinterließ eine Menge des Metalls zum Verkauf bei einem Mineralhändler in der Gerrard Street, London, und veröffentlichte anonym Handzettel in der ganzen Stadt, Beschreibung der Eigenschaften des neuen Metalls.,
Der Verdacht auf diese ungewöhnliche Herstellungsmethode entstand und Richard Chenevix, ein berühmter Chemiker zu der Zeit, erklärte Palladium zu einer Platin-Quecksilber-Legierung. (2)
Als Antwort darauf bot Wollaston jedem, der Palladium künstlich produzieren konnte, anonym eine Belohnung von zwanzig Guineen an. Niemand hat jemals dieses Geld beansprucht.
1805 sprach Wollaston vor der Royal Society of London über die Eigenschaften von Palladium und wie es von Platin isoliert werden konnte. Er beendete seinen Vortrag, indem er sich als Entdecker von Palladium offenbarte.,
Er erklärte, dass er anonym geblieben sei, damit er die Zeit habe, alle Eigenschaften des Metalls zu verstehen und zu erklären, bevor er seinen Namen auf ein Konto bringe. (3)
Das Element ist nach dem vor kurzem entdeckten Asteroiden Pallas benannt. Der Name des Asteroiden bezieht sich auf die antike griechische Göttin der Weisheit., (4)


Es ist möglich, dass eine Reihe von Erdmetallen von Asteroiden und anderen Planeten Kometeneinschlag nachdem sich der Planet bereits gebildet hatte, erklärt, warum die dichten Metalle Palladium, Gold und Platin relativ nahe an der Oberfläche unseres Planeten verfügbar sind. Bild von der NASA.
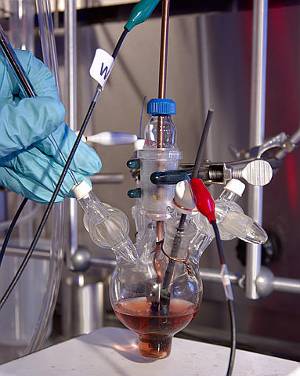
Palladium wird Häufig als Katalysator eingesetzt., Hier wird es verwendet, um die Reduktion von Kohlendioxid zu Kohlenmonoxid zu katalysieren. Bild von PNL.
Aussehen und Eigenschaften
Schädliche Wirkungen:
Palladium gilt als von geringer Toxizität.
Eigenschaften:
Palladium ist ein seltenes, glänzendes, silbrig-weißes Metall.
Es ist eines der sechs Platingruppenmetalle, bestehend aus Platin, Palladium, Rhodium, Osmium, Iridium und Ruthenium.
Die Metalle der Platingruppe
Diese Metalle haben ähnliche Eigenschaften und sind oft in den gleichen mineralischen Erzen vorhanden.,
| 44 Ru |
45 Rh |
46 Pd |
| 76 Os |
77 Ir |
78 Pt |
Palladium ist hämmerbar und duktil und wie gold, ist es, die geschlagen werden kann, in dünne Blätter.
Es trübt nicht an der Luft, sondern trübt leicht in feuchter schwefelhaltiger Luft.
Das Metall ist bei normalen Temperaturen stark korrosionsbeständig in der Luft und gegenüber Säuren (außer Salpetersäure).,
Wenn Palladium in Verbindungen vorhanden ist, existiert es hauptsächlich im Oxidationszustand II.
Palladium ist bemerkenswert in seiner Fähigkeit, bis zum 900-fachen seines eigenen Wasserstoffvolumens zu absorbieren. Wenn es den Wasserstoff absorbiert, dehnt es sich sichtbar aus, wie ein Schwamm, der beim Aufnehmen von Wasser aufquillt.
Verwendung von Palladium
Der größte Einsatz von Palladium findet in Katalysatoren für Automobile statt.
Feinteiliges Palladium wird als Katalysator für Hydrier – /Dehydrierungsreaktionen und für Erdölrisse verwendet.,
Das Metall wird in Schmuck verwendet, beispielsweise in Weißgold (einer Legierung aus Gold, die durch Zugabe von Palladium entfärbt wird).
Palladium wird in der Zahnmedizin, in der Uhrenherstellung und bei der Herstellung chirurgischer Instrumente und elektrischer Kontakte verwendet.
Es wird auch zur Reinigung von Wasserstoff verwendet, da das Gas leicht durch erhitztes Palladium diffundiert.,
Fülle und Isotope
Fülle Erdkruste: 15 Teile pro Milliarde Gewicht, 2 Teile pro Milliarde Mol
Fülle Sonnensystem: 3 Teile pro Milliarde Gewicht, 40 Teile pro Billion Mol
Kosten, rein: 5833 USD pro 100 g
Kosten, Bulk: 1571 USD pro 100 g
Quelle:Palladium kommt in der Natur als freies Metall vor und wird auch mit Gold, Platin und anderem Platin legiert gruppe Metalle. Kommerziell wird es aus Nickel–Kupfer-Erzvorkommen hergestellt, wo es in kleinen Mengen vorkommt.,

- Foto von PNNL
- Thomas Holz, Die Wirkung von Kohlenstoff auf Palladium: Inaug. Diss. von der Georgia-Augusta-Universität Göttingen, 1859, T. Chapman Browne, p4-6
- R. Hastings, Der Chemiker, Band 7, 1846, George Peirce., p388-389
- Mary Elvira Wochen, Die Entdeckung der Elemente VIII. Die Platin-Metalle, Journal of Chemical Education., Juni 1932, S. 102.,
Zitieren Sie diese Seite
Für die Online-Verknüpfung kopieren und fügen Sie bitte eine der folgenden ein:
<a href="https://www.chemicool.com/elements/palladium.html">Palladium</a>
oder
<a href="https://www.chemicool.com/elements/palladium.html">Palladium Element Facts</a>
Um diese Seite in einem akademischen Dokument zu zitieren, verwenden Sie bitte das folgende MLA-konforme Zitat:
"Palladium." Chemicool Periodic Table. Chemicool.com. 17 Oct. 2012. Web. <https://www.chemicool.com/elements/palladium.html>.