Pharmakotherapeutische Gruppe: Arzneimittel zur Behandlung von Diabetes, blutzuckersenkende Arzneimittel, ausgenommen Insuline. ATC-code: A10BK02.
Wirkmechanismus
Der in den proximalen Nierentubuli exprimierte SGLT2-Transporter ist für den Großteil der Reabsorption von gefilterterter Glukose aus dem tubulären Lumen verantwortlich., Es wurde gezeigt, dass Patienten mit Diabetes eine erhöhte renale Glukoserückresorption aufweisen, die zu anhaltend erhöhten Blutzuckerkonzentrationen beitragen kann. Canagliflozin ist ein oral aktiver Inhibitor von SGLT2. Durch die Hemmung von SGLT2 reduziert Canagliflozin die Reabsorption von gefilterterter Glukose und senkt die Nierenschwelle für Glukose (RTG) und erhöht dadurch die UGE, wodurch erhöhte Plasmaglukosekonzentrationen durch diesen insulinunabhängigen Mechanismus bei Patienten mit Typ-2-Diabetes gesenkt werden., Die erhöhte UGE mit SGLT2-Hemmung führt auch zu einer osmotischen Diurese, wobei die harntreibende Wirkung zu einer Senkung des systolischen Blutdrucks führt; Der Anstieg der UGE führt zu einem Kalorienverlust und damit zu einer Verringerung des Körpergewichts, wie in Studien an Patienten mit Typ-2-Diabetes gezeigt wurde.
Die Wirkung von Canagliflozin zur Erhöhung der UGE, die die Plasmaglukose direkt senkt, ist unabhängig von Insulin., In klinischen Studien mit Canagliflozin wurde eine Verbesserung der Homöostase-Modellbewertung für die Beta-Zell-Funktion (HOMA Beta-Cell) und eine verbesserte Reaktion der Beta-Zell-Insulinsekretion auf eine Herausforderung durch gemischte Mahlzeiten beobachtet.
In Phase-3-Studien führte die Verabreichung von Canagliflozin 300 mg vor der Mahlzeit zu einer stärkeren Verringerung der postprandialen Glukosekonzentration als bei der 100-mg-Dosis beobachtet., Dieser Effekt bei der 300-mg-Dosis von Canagliflozin kann zum Teil auf eine lokale Hemmung des intestinalen SGLT1 (eines wichtigen intestinalen Glukosetransporters) zurückzuführen sein, die mit vorübergehenden hohen Konzentrationen von Canagliflozin im Darmlumen vor der Resorption von Arzneimitteln zusammenhängt (Canagliflozin ist ein Inhibitor mit geringer Wirksamkeit des SGLT1-Transporters). Studien haben keine Glucose-Malabsorption mit Canagliflozin gezeigt.,
Canagliflozin erhöht die Abgabe von Natrium an den distalen Tubulus, indem es die SGLT2-abhängige Glukose-und Natriumreabsorption blockiert, wodurch die tubuloglomeruläre Rückkopplung erhöht wird, was mit einer Verringerung des intra-glomerulären Drucks und einer Abnahme der Hyperfiltration in präklinischen Modellen von Diabetes und klinischen Studien verbunden ist.
Pharmakodynamische Wirkungen
Nach Einzel-und Mehrfachdosen von Canagliflozin bei Patienten mit Typ-2-Diabetes wurden dosisabhängige RTG-Abnahmen und UGE-Erhöhungen beobachtet., Ab einem Anfangswert von RTG von ungefähr 13 mmol/l wurde bei Patienten mit Typ-2-Diabetes in Phase-1-Studien eine maximale Unterdrückung der 24-Stunden-RTG mit einer Tagesdosis von 300 mg auf ungefähr 4 mmol/l bis 5 mmol / l beobachtet, was auf ein geringes Risiko für eine behandlungsinduzierte Hypoglykämie hindeutet. Die Verringerung der RTG führte zu einer erhöhten UGE bei Patienten mit Typ-2-Diabetes, die in den Phase-1-Studien entweder mit 100 mg oder 300 mg Canagliflozin von 77 g/Tag bis 119 g/Tag behandelt wurden; Die beobachtete UGE führt zu einem Verlust von 308 kcal/Tag bis 476 kcal/Tag., Die Verringerung der RTG und die Erhöhung der UGE wurden über einen Zeitraum von 26 Wochen bei Patienten mit Typ-2-Diabetes aufrechterhalten. Moderate Anstiege (im Allgemeinen < 400 ml auf 500 ml) im täglichen Urinvolumen wurden beobachtet, die über mehrere Tage der Dosierung abgeschwächt wurden. Die Harnsäureausscheidung im Urin wurde vorübergehend durch Canagliflozin erhöht (Anstieg um 19% im Vergleich zum Ausgangswert am Tag 1 und dann Abschwächung auf 6% am Tag 2 und 1% am Tag 13). Dies ging einher mit einer anhaltenden Verringerung der Serumharnsäurekonzentration um etwa 20%.,
In einer Einzeldosis-Studie bei Patienten mit Typ-2-Diabetes verzögerte die Behandlung mit 300 mg vor einer gemischten Mahlzeit die intestinale Glukoseabsorption und reduzierte die postprandiale Glukose sowohl durch einen Nieren-als auch durch einen nicht-renalen Mechanismus.
Klinische Wirksamkeit und Sicherheit
Verbesserung der Blutzuckerkontrolle und Verringerung der kardiovaskulären und renalen Morbidität und Mortalität sind integraler Bestandteil der Behandlung von Typ-2-Diabetes.,
Glykämische Wirksamkeit und Sicherheit
Insgesamt 10.501 Patienten mit Typ-2-Diabetes nahmen an zehn doppelblinden, kontrollierten klinischen Wirksamkeits-und Sicherheitsstudien teil, die zur Bewertung der Auswirkungen von Invokana auf die glykämische Kontrolle durchgeführt wurden. Die Rassenverteilung betrug 72% Weiße, 16% asiatische, 5% schwarze und 8% andere Gruppen. 17% der Patienten waren hispanisch. 58% der Patienten waren Männlich. Die Patienten hatten ein Gesamtmittelalter von 59, 5 Jahren (Bereich 21 Jahre bis 96 Jahre), wobei 3.135 Patienten ≥ 65 Jahre und 513 Patienten ≥ 75 Jahre alt waren. 58% der Patienten hatten einen body-mass-index (BMI) ≥ 30 kg/m2., Im klinischen Entwicklungsprogramm, 1,085 Patienten mit einer baseline-eGFR von 30 mL/min/1,73 m2 bis < 60 mL/min/1,73 m2 untersucht.
placebokontrollierte Studien
Canagliflozin wurde als Monotherapie, Doppeltherapie mit Metformin, Doppeltherapie mit Sulfonylharnstoff, Dreifachtherapie mit Metformin und Sulfonylharnstoff, Dreifachtherapie mit Metformin und Pioglitazon sowie als Zusatztherapie mit Insulin untersucht (Tabelle 4). Im Allgemeinen, canagliflozin produziert klinisch und statistisch signifikant (p < 0.,001) Ergebnisse im Vergleich zu Placebo bei der glykämischen Kontrolle, einschließlich HbA1c, der Prozentsatz der Patienten, die HbA1c < 7% erreichen, Veränderung gegenüber der Basislinie Fasten Plasmaglukose (FPG) und 2-Stunden-postprandiale Glukose (PPG). Darüber hinaus wurden eine Verringerung des Körpergewichts und des systolischen Blutdrucks im Vergleich zu Placebo beobachtet.,
Darüber hinaus wurde Canagliflozin als Dreifachtherapie mit Metformin und Sitagliptin untersucht und mit einem Titrationsschema dosiert, wobei eine Anfangsdosis von 100 mg verwendet und bereits in Woche 6 auf 300 mg titriert wurde Patienten, die eine zusätzliche glykämische Kontrolle erforderten, die über eine geeignete eGFR verfügten und Canagliflozin 100 mg vertragen (Tabelle 4). Canagliflozin, das mit einem Titrationsschema dosiert wurde, erzeugte klinisch und statistisch signifikant (p < 0.,001) Ergebnisse im Vergleich zu Placebo bei der glykämischen Kontrolle, einschließlich HbA1c und Veränderung gegenüber dem Ausgangsfastenplasma Glucose (FPG), und eine statistisch signifikante (p < 0.01) Verbesserung des Prozentsatzes der Patienten, die HbA1c < 7% erreichen. Darüber hinaus wurden eine Verringerung des Körpergewichts und des systolischen Blutdrucks im Vergleich zu Placebo beobachtet.,
Zusätzlich zu den oben vorgestellten Studien waren die Ergebnisse der glykämischen Wirksamkeit, die in einer 18-wöchigen dualen Therapieteilstudie mit Sulfonylharnstoff und einer 26-wöchigen Dreifachtherapiestudie mit Metformin und Pioglitazon beobachtet wurden, im Allgemeinen vergleichbar mit denen, die in anderen Studien beobachtet wurden.
Aktiv-kontrollierte Studien
Canagliflozin wurde mit Glimepirid als duale Therapie mit Metformin und mit Sitagliptin als Dreifachtherapie mit Metformin und Sulfonylharnstoff verglichen (Tabelle 5)., Canagliflozin 100 mg als Doppeltherapie mit Metformin führte zu ähnlichen Reduktionen von HbA1c gegenüber dem Ausgangswert und 300 mg zu überlegenen (p < 0,05) Reduktionen von HbA1c im Vergleich zu Glimepirid, was eine Nicht-Minderwertigkeit zeigt. Ein geringerer Anteil der Patienten, die mit Canagliflozin 100 mg (5,6%) und Canagliflozin 300 mg (4,9%) behandelt wurden, erlebte mindestens eine Episode/ein Ereignis von Hypoglykämie über 52 Wochen der Behandlung im Vergleich zu der mit Glimepirid behandelten Gruppe (34,2%)., In einer Studie, in der Canagliflozin 300 mg mit Sitagliptin 100 mg in Dreifachtherapie mit Metformin und einem Sulfonylharnstoff verglichen wurde, zeigte Canagliflozin eine nicht minderwertige (p < 0,05) und überlegene (p < 0,05) Reduktion von HbA1c im Vergleich zu Sitagliptin. Die Inzidenz von Hypoglykämieepisoden / Ereignissen mit Canagliflozin 300 mg und Sitagliptin 100 mg betrug 40,7% bzw. Signifikante Verbesserungen des Körpergewichts und eine Senkung des systolischen Blutdrucks im Vergleich zu Glimepirid und Sitagliptin wurden ebenfalls beobachtet.,
Canagliflozin als anfängliche Kombinationstherapie mit Metformin
Canagliflozin wurde in Kombination mit Metformin als anfängliche Kombinationstherapie bei Patienten mit Typ-2-Diabetes ohne Diät und Bewegung untersucht. Canagliflozin 100 mg und Canagliflozin 300 mg in Kombination mit Metformin XR führten zu einer statistisch signifikant größeren Verbesserung des HbA1c im Vergleich zu den jeweiligen Canagliflozin-Dosen (100 mg und 300 mg) allein oder Metformin XR allein (Tabelle 6).,
Spezielle Populationen
In drei Studien, die in speziellen Populationen durchgeführt wurden (ältere Patienten, Patienten mit einem eGFR von 30 ml/min/1,73 m2 bis < 50 ml/min/1,73 m2 und Patienten mit oder mit hohem Risiko für Herz-Kreislauf-Erkrankungen), wurde Canagliflozin zu den derzeit stabilen Diabetesbehandlungen der Patienten hinzugefügt (Diät, Monotherapie oder Kombinationstherapie).,
Ältere Menschen
Insgesamt 714 Patienten ≥ 55 Jahre bis ≤ 80 Jahre (227 Patienten 65 Jahre bis < 75 Jahre und 46 Patienten 75 Jahre bis ≤ 80 Jahre) mit unzureichender glykämischer Kontrolle der aktuellen Diabetesbehandlung (glukosesenkende Arzneimittel und/oder Diät und Bewegung) nahmen über 26 Wochen an einer doppelblinden, placebokontrollierten Studie teil. Statistisch signifikante (p < 0.001) Veränderungen gegenüber dem Ausgangswert HbA1c relativ zu Placebo von -0.57% und -0.,70% wurden für 100 mg bzw. 300 mg beobachtet (siehe Abschnitte 4.2 und 4.8).
Patienten mit eGFR 45 mL/min/1,73 m2 bis < 60 mL/min/1,73 m2
In einer gepoolten Analyse von Patienten (N = 721) mit einer baseline-eGFR 45 mL/min/1,73 m2 bis < 60 mL/min/1,73 m2, canagliflozin, sofern klinisch bedeutsamen Reduktion des HbA1c im Vergleich zu placebo, mit -0.47% für canagliflozin 100 mg und -0.52% für canagliflozin 300 mg. Patienten mit einer baseline-eGFR 45 mL/min/1,73 m2 bis < 60 mL/min/1.,73 m2, die mit Canagliflozin 100 mg und 300 mg behandelt wurden, zeigten eine durchschnittliche prozentuale Veränderung des Körpergewichts im Vergleich zu Placebo von -1,8% bzw.
Die Mehrzahl der Patienten mit einem Ausgangswert eGFR 45 ml / min / 1,73 m2 bis < 60 mL/min/1,73 m2 erhielten Insulin und / oder Sulfonylharnstoff (85% )., In Übereinstimmung mit dem erwarteten Anstieg der Hypoglykämie, wenn ein Arzneimittel, das nicht mit Hypoglykämie assoziiert ist, Insulin und/oder Sulfonylharnstoff zugesetzt wird, wurde ein Anstieg der Hypoglykämie-Episoden/ – Ereignisse beobachtet, wenn Canagliflozin Insulin und/oder Sulfonylharnstoff zugesetzt wurde (siehe Abschnitt 4.8).
Nüchternplasmaglukose
In vier placebokontrollierten Studien führte die Behandlung mit Canagliflozin als Monotherapie oder Ergänzungstherapie mit einem oder zwei oralen glukosesenkenden Arzneimitteln zu mittleren Veränderungen gegenüber dem Ausgangswert im Vergleich zu Placebo in FPG von -1, 2 mmol/l bis -1.,9 mmol/l für Canagliflozin 100 mg und -1,9 mmol/l bis -2,4 mmol / l für Canagliflozin 300 mg. Diese Reduktionen wurden über den Behandlungszeitraum und nahezu maximal nach dem ersten Behandlungstag aufrechterhalten.
Postprandiale Glukose
Unter Verwendung eines Mixed-Meal-Arzneimittels reduzierte Canagliflozin als Monotherapie oder Zusatztherapie mit einem oder zwei oralen glukosesenkenden Arzneimitteln die postprandiale Glukose (PPG) vom Ausgangswert im Vergleich zu Placebo um -1,5 mmol/l auf -2,7 mmol/l für Canagliflozin 100 mg und -2,1 mmol/L auf -3.,5 mmol / l für 300 mg aufgrund einer Verringerung der Glukosekonzentration vor dem Essen und einer verringerten postprandialen Glukosekonzentration.
Körpergewicht
Canagliflozin 100 mg und 300 mg als Monotherapie und als duale oder dreifache Zusatztherapie führten zu einer statistisch signifikanten Verringerung des Körpergewichtsanteils nach 26 Wochen im Vergleich zu Placebo., In zwei 52-wöchigen aktiv kontrollierten Studien, in denen Canagliflozin mit Glimepirid und Sitagliptin verglichen wurde, betrug die anhaltende und statistisch signifikante mittlere Verringerung des Körpergewichtsprozentsatzes für Canagliflozin als Zusatztherapie zu Metformin -4,2% und -4,7% für Canagliflozin 100 mg bzw. Sulfonylharnstoff im Vergleich zu Sitagliptin in Kombination mit Metformin und einem Sulfonylharnstoff (0,3%).,
Eine Untergruppe von Patienten (N = 208) aus der aktiv-kontrollierten Dualtherapiestudie mit Metformin, die sich einer dualen Energie-Röntgendensitometrie (DXA) und einer abdominalen Computertomographie (CT) zur Beurteilung der Körperzusammensetzung unterzog, zeigte, dass etwa zwei Drittel des Gewichtsverlusts mit Canagliflozin auf den Verlust von Fettmasse zurückzuführen waren, wobei ähnliche Mengen an viszeralem und abdominalem subkutanem Fett verloren gingen. Zwei hundert elf (211) Patienten aus der klinischen Studie bei älteren Patienten teilgenommen, die in einem Körper Zusammensetzung substudy mit DXA-body-composition-Analyse., Dies zeigte, dass etwa zwei Drittel des mit Canagliflozin verbundenen Gewichtsverlusts auf den Verlust von Fettmasse im Vergleich zu Placebo zurückzuführen waren. Es gab keine signifikanten Veränderungen der Knochendichte in trabekulären und kortikalen Regionen.
Blutdruck
In placebokontrollierten Studien führte die Behandlung mit Canagliflozin 100 mg und 300 mg zu einer mittleren Senkung des systolischen Blutdrucks von -3,9 mmHg bzw. -5,3 mmHg im Vergleich zu Placebo (-0,1 mmHg)und einer geringeren Wirkung auf den diastolischen Blutdruck mit mittleren Veränderungen für Canagliflozin 100 mg und 300 mg -2,1 mmHg und -2.,5 mmHg im Vergleich zu Placebo (-0,3 mmHg). Es gab keine nennenswerte Änderung der Herzfrequenz.
Patienten mit HbA1c-Ausgangswert > 10% bis ≤ 12%
Eine Untergruppe von Patienten mit HbA1c-Ausgangswert > 10% bis ≤ 12% mit Canagliflozin als Monotherapie führte zu einer Verringerung des HbA1c-Ausgangswerts (nicht Placebo-angepasst) von -2,13% und -2,56% bei Canagliflozin 100 mg und 300 mg.beziehungsweise.,
Kardiovaskuläre Ergebnisse im CANVAS-Programm
Die Wirkung von Canagliflozin auf kardiovaskuläre Ereignisse bei Erwachsenen mit Typ-2-Diabetes, bei denen eine kardiovaskuläre Erkrankung (CV) festgestellt wurde oder ein Risiko für CVD (zwei oder mehr CV-Risikofaktoren) bestand, wurde im CANVAS-Programm bewertet (integrierte Analyse des CANVAS und der CANVAS-R-Studie). Diese Studien waren multizentrisch, multinational, randomisiert, doppelblind, Parallelgruppe, mit ähnlichen Einschluss-und Ausschlusskriterien und Patientenpopulationen., Das CANVAS-Programm verglich das Risiko eines schwerwiegenden unerwünschten kardiovaskulären Ereignisses (Streitkolben), das als Zusammengesetzt aus kardiovaskulärem Tod, nicht tödlichem Myokardinfarkt und nicht tödlichem Schlaganfall definiert ist, zwischen Canagliflozin und Placebo vor dem Hintergrund von Standardbehandlungen für Diabetes und atherosklerotische Herz-Kreislauf-Erkrankungen.
In CANVAS wurden den Probanden nach dem Zufallsprinzip 1:1:1 Canagliflozin 100 mg, Canagliflozin 300 mg oder passendes Placebo zugewiesen., In CANVAS-R wurden den Probanden nach dem Zufallsprinzip 1:1 Canagliflozin 100 mg oder ein passendes Placebo zugewiesen, und eine Titration auf 300 mg war (basierend auf Verträglichkeit und glykämischem Bedarf) nach Woche 13 zulässig. Begleitende antidiabetische und atherosklerotische Therapien könnten entsprechend der Standardversorgung für diese Krankheiten angepasst werden.
Insgesamt wurden 10,134 Patienten behandelt (4,327 in CANVAS und 5,807 in CANVAS-R; insgesamt 4,344 zufällig Placebo und 5,790 Canagliflozin zugeordnet) für eine mittlere Expositionsdauer von 149 Wochen (223 Wochen in CANVAS und 94 Wochen in CANVAS-R). Vitalstatus wurde für 99 erhalten.,6% der Probanden über die Studien. Das Durchschnittsalter betrug 63 Jahre und 64% waren männlich. Sechsundsechzig Prozent der Probanden hatten eine Vorgeschichte etablierter kardiovaskulärer Erkrankungen, wobei 56% eine Vorgeschichte von Koronarerkrankungen hatten, 19% mit zerebrovaskulären Erkrankungen und 21% mit peripheren Gefäßerkrankungen; 14% hatten eine Vorgeschichte von Herzinsuffizienz.
Der mittlere HbA1c zu Studienbeginn betrug 8,2% und die mittlere Diabetesdauer 13,5 Jahre.
Die Nierenfunktion war bei 80% der Patienten normal oder leicht beeinträchtigt und bei 20% der Patienten mäßig beeinträchtigt (mittlerer eGFR 77 ml/min/1, 73 m2)., Zu Studienbeginn wurden die Patienten mit einem oder mehreren Antidiabetika wie Metformin (77%), Insulin (50%) und Sulfonylharnstoff (43%) behandelt.
Der primäre Endpunkt im CANVAS-Programm war die Zeit bis zum ersten Auftreten eines Streitkolbens. Sekundäre Endpunkte innerhalb eines sequentiellen bedingten Hypothesentests waren Mortalität und kardiovaskuläre Mortalität.
Patienten in den gepoolten Canagliflozin-Gruppen (gepoolte Analyse von Canagliflozin 100 mg, Canagliflozin 300 mg und Canagliflozin up-titriert von 100 mg bis 300 mg) hatten im Vergleich zu Placebo eine niedrigere Streitkolbenrate: 2, 69 gegenüber 3.,15 patienten pro 100 Patientenjahre (HR der gepoolten Analyse: 0,86; 95% CI (0,75, 0,97).
Basierend auf dem Kaplan-Meier-Diagramm für das erste Auftreten von Streitkolben (siehe unten) wurde die Verringerung der STREITKOLBEN in der Canagliflozin-Gruppe bereits in Woche 26 beobachtet und während des gesamten Rests der Studie beibehalten (siehe Abbildung 1).
Abbildung 1: Zeit bis zum ersten auftreten von MACE
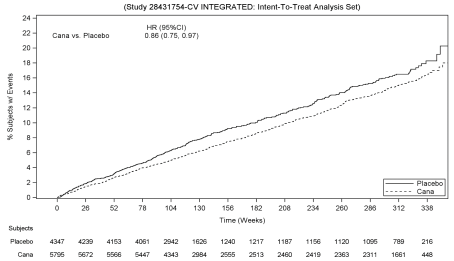
Es wurden 2,011 Patienten mit eGFR 30 bis < 60 mL/min/1,73 m2. Die KEULE Ergebnisse in dieser Untergruppe wurden im Einklang mit dem generellen Befund.,
Jede Streitkolbenkomponente trug positiv zum Gesamtverbund bei, wie in Abbildung 2 gezeigt. Die Ergebnisse für die Dosen von 100 mg und 300 mg Canagliflozin stimmten mit den Ergebnissen für die kombinierten Dosisgruppen überein.
Abbildung 2: Behandlungseffekt für den primären zusammengesetzten Endpunkt und seine Komponenten
1 P Wert für Überlegenheit (2-seitig) = 0,0158.
Gesamtmortalität im CANVAS-Programm
In der kombinierten Canagliflozin-Gruppe betrug die HR für Gesamtmortalität gegenüber Placebo 0,87; 95% CI (0,74, 1,01).,
Herzinsuffizienz, die einen Krankenhausaufenthalt im CANVAS-Programm erfordert
Canagliflozin reduzierte das Risiko für eine Krankenhauseinweisung erfordernde Herzinsuffizienz im Vergleich zu Placebo (HR: 0, 67; 95% CI (0, 52, 0, 87)).
Renale Endpunkte im CANVAS-Programm
Renale Ergebnisse in der CREDENCE-Studie
Die Wirkung von Canagliflozin 100 mg auf Nierenereignisse bei Erwachsenen mit Typ-2-Diabetes und diabetischer Nierenerkrankung (DKD) mit geschätzter glomerulärer Filtrationsrate (eGFR) 30 bis < 90 ml/min/1.,73 m2 und Albuminurie (300 bis 5000 mg/g Kreatinin) wurden in der Canagliflozin-und Nierenerkrankung bei Diabetes mit etablierter klinischer Nephropathie-Evaluierungsstudie (CREDENCE) untersucht. Dies war eine multizentrische, multinationale, randomisierte, doppelblinde, ereignisgesteuerte, placebokontrollierte Parallelgruppenstudie., Die CREDENCE-Studie verglich das Risiko einer DKD, definiert als die Kombination von Nierenerkrankungen im Endstadium, einer Verdoppelung des Serumkreatinin und einem nieren-oder kardiovaskulären Tod, zwischen Canagliflozin 100 mg und Placebo vor dem Hintergrund von Standardbehandlungen für DKD, einschließlich Angiotensin-Converting-Enzym-Inhibitor (ACEi) oder Angiotensin-Rezeptor-Blocker (ARB). Canagliflozin 300 mg wurde in dieser Studie nicht untersucht.,
In den GLAUBEN die Probanden wurden randomisiert 1:1 zu canagliflozin 100 mg oder placebo, geschichtet durch das screening von eGFR 30 bis <45, 45 bis <60 60 bis <90 mL/min/1,73 m2. Die Behandlung mit Canagliflozin 100 mg wurde bei Patienten bis zum Beginn der Dialyse oder im Falle einer Nierentransplantation fortgesetzt.
insgesamt 4,397 Themen wurden behandelt und ausgesetzt, für die ein Mittelwert von 115 Wochen. Das Durchschnittsalter betrug 63 Jahre und 66% waren männlich.
Die mittlere Baseline HbA1c war 8.,3% und der mediane Ausgangsurinalbumin / Kreatinin betrug 927 mg / g. Die häufigsten zu Studienbeginn verwendeten antihyperglykämischen Mittel (AHA) waren Insulin (65, 5%), Biguanide (57, 8%) und Sulfonylharnstoffe (28, 8%). Fast alle Probanden (99,9%) waren randomisiert an ACEi oder ARB beteiligt. Etwa 92% der Probanden erhielten zu Studienbeginn kardiovaskuläre Therapien (ohne ACEi/ARBs), wobei etwa 60% ein antithrombotisches Mittel (einschließlich Acetylsalicylsäure) und 69% Statine einnahmen.
Die mittlere baseline-eGFR war 56.2 mL/min/1.,73 m2 und rund 60% der Bevölkerung hatten eine baseline-eGFR von < 60 mL/min/1,73 m2. Der Anteil der Probanden mit vorheriger CV-Erkrankung betrug 50,4%; 14,8% hatten eine Herzinsuffizienz in der Vorgeschichte.
Der primäre zusammengesetzte Endpunkt in der CREDENCE-Studie war die Zeit bis zum ersten Auftreten von ESKD (definiert als eGFR < 15 ml/min/1.73 m2, Beginn einer chronischen Dialyse oder Nierentransplantation), Verdoppelung des Serumkreatinin und Nieren-oder CV-Tod.,
Canagliflozin 100 mg reduzierte signifikant das Risiko des ersten Auftretens des primären Kompositendpunkts von ESKD, der Verdoppelung des Serumkreatinin und des Nieren-oder CV-Todes (siehe Abbildung 4). Der Behandlungseffekt war in allen Untergruppen konsistent, einschließlich aller drei eGFR-Schichten und Probanden mit oder ohne CV-Erkrankung in der Vorgeschichte.
Basierend auf dem Kaplan-Meier-Plot für die Zeit bis zum ersten Auftreten des unten gezeigten primären zusammengesetzten Endpunkts war der Behandlungseffekt ab Woche 52 mit Canagliflozin 100 mg offensichtlich und wurde bis zum Ende der Studie aufrechterhalten (siehe Abbildung 3).,
Canagliflozin 100 mg reduzierte das Risiko kardiovaskulärer sekundärer Endpunkte signifikant, wie in Abbildung 4 gezeigt.
Abbildung 3: GLAUBWÜRDIGKEIT: Zeit bis zum ersten Auftreten des primären zusammengesetzten Endpunkts
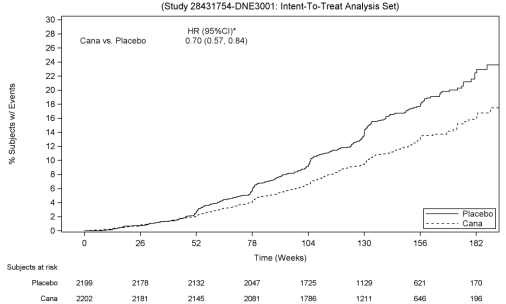
* 95% RCI (Wiederholtes Konfidenzintervall) für den primären Endpunkt mit familienweiser Fehlerrate vom Typ I, die auf einem 2-seitigen Signifikanzniveau von 0,05 gesteuert wird.,
Abbildung 4: Behandlungseffekt für den primären zusammengesetzten Endpunkt und seine Komponenten und sekundären Endpunkte
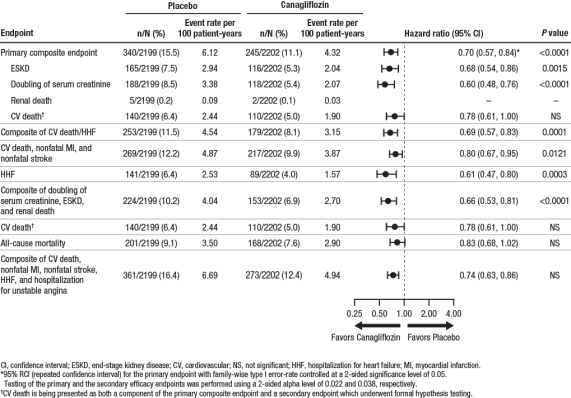
Wie in Abbildung 5 gezeigt, zeigte die eGFR bei Placebo-behandelten Patienten einen progressiven linearen Rückgang im Laufe der Zeit; Im Gegensatz dazu zeigte die Canagliflozin-Gruppe in Woche 3 eine akute Abnahme, gefolgt von einem abgeschwächten Rückgang im Laufe der Zeit; Nach Woche 52 war die LS-mittlere Abnahme der eGFR in der Canagliflozin-Gruppe in der Placebo-Gruppe, und der Behandlungseffekt wurde bis zum Ende der Behandlung beibehalten.,
Abbildung 5: LS mittlere Veränderung gegenüber dem Ausgangswert der eGFR im Laufe der Zeit (On-Treatment-Analyseset)
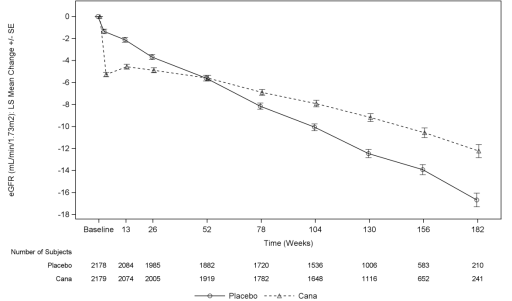
In CREDENCE war die Inzidenzrate für nierenbedingte unerwünschte Ereignisse in der Canagliflozin 100 mg-Gruppe im Vergleich zur Placebo-Gruppe niedriger (5,71 und 7,91 pro 100 Patientenjahre in Canagliflozin 100 mg bzw.
Pädiatrische Population
Die Europäische Arzneimittel-Agentur hat die Verpflichtung zur Vorlage der Ergebnisse von Studien mit Canagliflozin in einer oder mehreren Untergruppen der pädiatrischen Population bei Typ-2-Diabetes aufgeschoben (siehe Abschnitt 4.,2 für Informationen zur pädiatrischen Anwendung).